Großbritannien warnt Menschen mit schweren Allergien, den Pfizer COVID-19-Impfstoff zu vermeiden Gesundheitsinfo
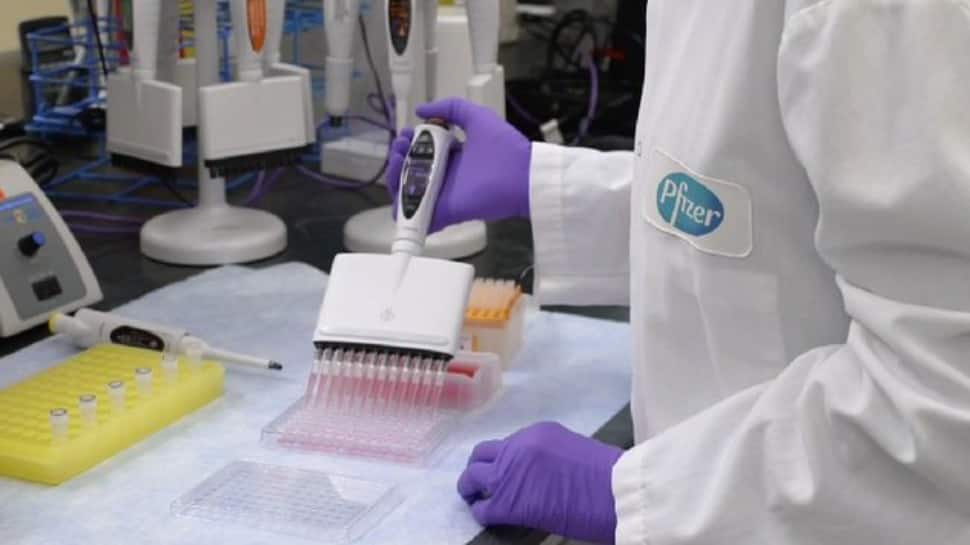
LONDON: Die britische Arzneimittelbehörde hat mitgeteilt, dass Personen mit einer Vorgeschichte signifikanter allergischer Reaktionen den COVID-19-Impfstoff von Pfizer-BioNTech nicht erhalten, nachdem zwei Personen am ersten Tag des Einsatzes Nebenwirkungen gemeldet hatten.
Großbritannien hat am Dienstag im Rahmen einer globalen Kampagne, die eine der größten logistischen Herausforderungen in der Geschichte des Friedens darstellt, mit der Massenimmunisierung seiner Bevölkerung begonnen, angefangen bei älteren Menschen und Arbeitern in der ersten Reihe.
Stephen Powis, medizinischer Direktor des Nationalen Gesundheitsdienstes, sagte, der Rat sei geändert worden, nachdem zwei NHS-Mitarbeiter anaphylaktoide Reaktionen im Zusammenhang mit dem Erhalt des Impfstoffs gemeldet hatten.
„Wie so oft bei neuen Impfstoffen hat die MHRA (Regulierungsbehörde) als vorbeugende Maßnahme empfohlen, dass Personen mit einer signifikanten Vorgeschichte allergischer Reaktionen diese Impfung nicht erhalten sollten, nachdem zwei Personen mit einer Vorgeschichte allergischer Reaktionen schwere Allergiker reagiert haben negativ gestern “, sagte Powis.
„Beide erholen sich gut.“
Die MHRA sagte, sie werde weitere Informationen einholen, und Pfizer und BioNTech sagten, sie unterstützten die Untersuchung der MHRA.
Die Regulierungsbehörde für Arzneimittel und Gesundheitsprodukte (MHRA) war die weltweit erste, die den von BioNTech und Pfizer in Deutschland entwickelten Impfstoff in der vergangenen Woche zugelassen hat, während die US-amerikanische Food and Drug Administration (FDA) und die European Medicines Agency (EMA) ) weiterhin die Daten auswerten.
„Letzte Nacht haben wir uns zwei Fallberichte über allergische Reaktionen angesehen. Wir wissen aus sehr umfangreichen klinischen Studien, dass dies kein Merkmal war“, sagte June Raine, CEO von MHRA, gegenüber dem Gesetzgeber.
Pfizer sagte, dass Menschen mit schwerwiegenden allergischen Nebenwirkungen in der Vorgeschichte von ihren Studien im Spätstadium ausgeschlossen wurden.
Die FDA veröffentlichte am Dienstag Dokumente zur Vorbereitung einer Sitzung des Beratungsausschusses am Donnerstag. Die Daten zur Wirksamkeit und Sicherheit des Pfizer-Impfstoffs entsprachen den Erwartungen für die Freigabe.
Nach diesem Hintergrund berichteten 0,63% der Personen in der geimpften Gruppe und 0,51% der Personen in der Placebogruppe über mögliche allergische Reaktionen in Studien, die laut Peter Openshaw, Professor für experimentelle Medizin am Imperial College London, sehr gering waren Nummer.
„Die Tatsache, dass wir so früh über diese beiden allergischen Reaktionen Bescheid wussten und dass die Regulierungsbehörde entsprechend gehandelt hat, um Vorsichtsmaßnahmen zu treffen, zeigt, dass dieses Überwachungssystem gut funktioniert“, sagte er.



